applications
Temps de lecture :Le domaine d’application de l’ozone est vaste du fait de sa forte réactivité (voir les oxydants et désinfectants). Dans le domaine du traitement de l’eau, il s’étend de la production d’eau de consommation à l’épuration d’eaux résiduaires industrielles.
en traitement des eaux de consommation
L’action de l’ozone est mise à profit à divers stades de production selon la qualité de l’eau à traiter. On trouvera au niveau des filières de traitement des eaux de surface, plusieurs tableaux et exemples d’application de l’ozone.
en préoxydation
En préoxydation, l’ozone est utilisé pour déstructurer les particules colloïdales et les macromolécules et améliorer ainsi les performances de la coagulation-floculation voire le fonctionnement de la décantation. L’eau clarifiée est de meilleure qualité en terme de turbidité et de matière organique (COT, composés précurseurs d’haloformes, composés responsables de goût et d’odeur). Il permet simultanément d’éliminer les algues présentes dans les eaux de surface. Il oxyde également le fer et le manganèse dans les eaux souterraines peu chargées en matière organique. La dose d’ozone appliquée à ce stade est voisine de 1 mg · L–1.
en oxydation intermédiaire ou principale
En oxydation intermédiaire ou principale, l’ozone a pour rôle d’oxyder les matières organiques dites naturelles. Il décolore les eaux chargées en substances humiques. Il transforme les composés organiques rencontrés tels que ceux responsables des goûts et des odeurs (par exemple, géosmine et 2-méthylisobornéol), les pesticides (glyphosate, aldicarb, pentachlorophénol…), les phénols, les détergents, les toxines algales et d’autres composés chimiques d’origine pharmaceutique et/ou à activité œstrogénique (par exemple, 17a- ethinylestradiol). Le degré de conversion de ces derniers varie selon leur structure chimique et les conditions du milieu. La voie de réactivité radicalaire notamment promue par l’addition de peroxyde d’hydrogène peut s’avérer nécessaire pour produire les taux d’élimination escomptés.
Ce type de procédé d’oxydation avancée est soumis à autorisation car les sous-produits formés peuvent entrer dans le périmètre de la réglementation (cas des pesticides et bromates en Europe). L’ozonation parvient en règle générale à diminuer la toxicité des composés dans l’eau et à augmenter leur biodégradabilité (CODB). En conséquence, l’ozonation principale est quasi-systématiquement couplée à une filtration biologique sur charbon actif en grains afin d’achever l’élimination des micropolluants tout en limitant la dose d’ozone appliquée. Celle-ci est en général de l’ordre de 0,5 à 1 g par g de carbone organique.
en désinfection
En désinfection, l’ozone réagit rapidement avec les micro-organismes de sorte que les valeurs de CT sont en général faibles (voir les oxydants et désinfectants). Les gammes de valeurs compilées à la figure 22 montrent que l’ozone est capable de détruire les principaux organismes pathogènes rencontrés. Malgré la dispersion des valeurs due à la variation des conditions expérimentales et des méthodes de dénombrement (excystation, infectivité) utilisées, il apparaît que :
- les micro-organismes les plus résistants sont les protozoaires tels que les kystes Naegleria et Cryptosporidium qui impliquent des CT plus de 100 fois supérieures à ceux nécessaires pour la bactérie E. coli ;
- un CT égal à 2 mg · min · L–1 est suffisant pour détruire à 99 % les bactéries, les virus et l’ensemble des kystes de Giardia.



Comme pour toute réaction chimique, l’action de l’ozone sur les micro-organismes dépend des conditions du milieu que sont le pH, la température, la présence d’autres composés oxydables et la concentration en MES. En effet :
- le pH conditionne la décomposition de l’ozone ; une augmentation de ce dernier vers des pH basiques a pour effet de réduire la concentration en ozone dissous et donc l’efficacité de désinfection ;
- bien que la température joue en sens inverse sur la solubilité de l’ozone et sur la vitesse d’inactivation, l’efficacité de désinfection augmente à température croissante (figure 23);
- les matières organiques contribuent à la demande en ozone de l’eau et entrent en compétition avec les micro-organismes (demande en ozone : voir analyses spécifiques). L’apparition d’ozone résiduel dissous dans l’eau ne se réalise que lorsque le taux d’oxydant introduit dépasse une valeur critique correspondant à la demande immédiate en ozone ;
- les matières en suspension peuvent protéger les micro-organismes et de ce fait rendre la désinfection plus difficile (vrai quel que soit l’agent désinfectant utilisé).

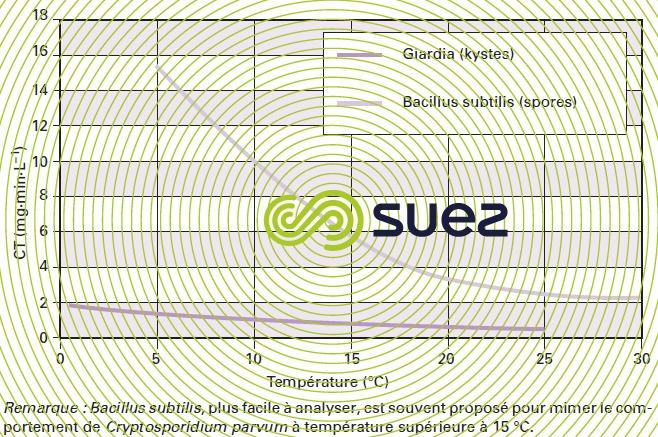

La valeur du CT à maintenir dépend des objectifs de désinfection. Il est admis que les conditions de traitement d’une eau potable fixées dès 1964 au taux de 0,4 mg · L–1 d’ozone résiduel pendant 4 minutes de temps de séjour (CT = 1,6 mg · min · L–1) satisfont à l’élimination de 2,5 log de kystes de Giardia lamblia à 5 °C. Les études les plus avancées concourent à montrer que l’inactivation d’un log de kystes de Cryptosporidium nécessiterait un CT égal à 4 mg · min · L–1 à 20 °C et égal à 10 mg · min · L–1 à 10 °C (compilation menée par USEPA). Dans ce contexte, l’application de l’ozone peut s’avérer non conforme vis-à-vis des normes en ion bromate (voir ci-après).


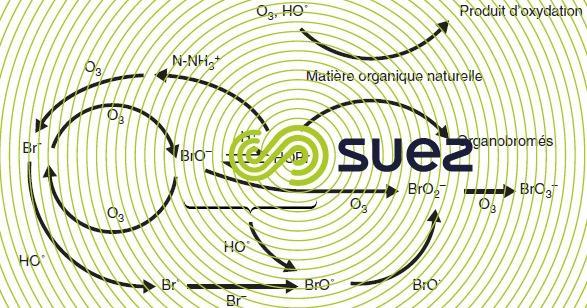
La formation de bromates au cours de l’ozonation résulte de l’oxydation des ions bromures selon un mécanisme complexe dans lequel l’ozone et le radical hydroxyle sont impliqués (figure 25). Dans les eaux naturelles de pH compris entre 6 et 8, l’ozone joue un rôle clé dans la formation de l’acide hypobromeux (HOBr) que le radical hydroxyle (HO•) oxyde ensuite en ion bromite (BrO2–) alors facilement converti en ion bromate (BrO3–) par l’ozone.
La formation de composés organobromés reste un phénomène minoritaire. Il s’ensuit que la conversion des bromures en bromates peut être minimisée moyennant :
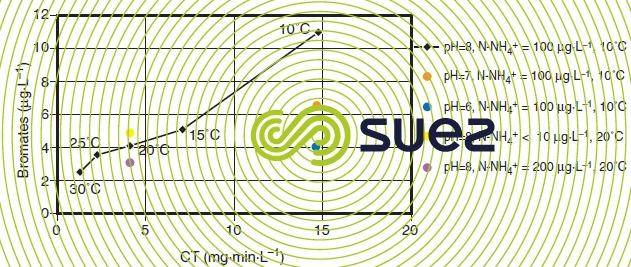
- le contrôle du pH pour limiter la décomposition de l’ozone en radical hydroxyle (voir les oxydants et désinfectants) et orienter l’équilibre HOBr/BrO– (figure 24, influence du pH pour CT = 15) ;
- l’addition d’ammoniaque qui réagit très rapidement avec l’acide hypobromeux ;
- la maîtrise de l’hydrodynamique du contacteur avec adaptation des conditions d’application de l’ozone.
L’évolution de la concentration en bromates peut être estimée connaissant la concentration initiale en bromures, la concentration en ozone dissous, le pH, la température et le temps de séjour.


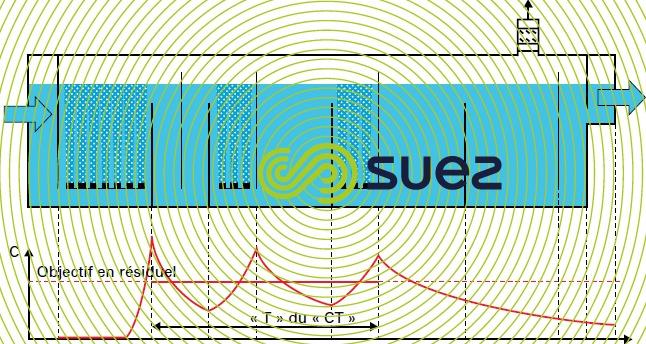
En production d’eau potable, les réacteurs d’ozonation principaux sont des chambres constituées de compartiments. Un seul compartiment avec un temps de contact de quelques minutes est en général suffisant pour assurer la préoxydation alors que pour l’oxydation principale et pour la désinfection, il est préférable d’utiliser des chambres à deux ou trois compartiments avec des temps de contact compris entre 8 et 15 minutes. Ces réacteurs sont dimensionnés en considérant que :
- le temps de séjour est correctement décrit par le modèle qui associe réacteurs agités pour chaque compartiment de diffusion du gaz et réacteurs piston entre les chicanes. L’efficacité hydrodynamique est évaluée en terme de T10 déterminé par traçage (voir applications) ;
- les paramètres cinétiques (demande immédiate en ozone, la vitesse ultérieure de consommation d’ozone en vue de l’obtention éventuelle d’une concentration résiduelle) sont connus soit via des tests de laboratoire soit par analogie.
Les bilans de matière sur l’ozone permettent alors de déterminer les valeurs de paramètres de fonctionnement que sont les débits gazeux dans chaque compartiment en fonction des caractéristiques géométriques et des contraintes opératoires (concentrations résiduelles recherchées pour l’ozone en désinfection, objectif de traitement en oxydation, voir illustration à la figure 26).


Le tube en U est également utilisé pour l’oxydation principale (photo 11). Le réacteur à diffuseur radial présenté à la figure 18 est également adapté en particulier à la préozonation.



eaux usées urbaines
L’application de l’ozone dans le domaine des eaux résiduaires répond à des objectifs variés.
Après traitement physico-chimique ou biologique, l’ozonation permet de :
- désinfecter les eaux traitées tout en diminuant la DCO résiduelle de 20 % au minimum avant réutilisation ou rejet dans les zones protégées ;
- décolorer et d’éliminer 4 à 8 mg · L–1 de détergents dans les eaux avec une dose d’ozone de l’ordre de 30 mg · L–1 (cas d’eaux ERU et ERI textile mélangées).
Les réacteurs sont principalement des chambres d’ozonation à compartiments conçues selon un principe analogue à celui adopté pour l’ozonation d’eau potable. En désinfection, les vitesses d’inactivation des bactéries ou virus étant très rapides et le maintien d’une concentration en ozone résiduel n’étant pas nécessaire, un temps de contact inférieur ou égal à deux minutes est suffisant pour la désinfection en chambre. Cette application se prête également à l’emploi de systèmes à mélangeur statique.
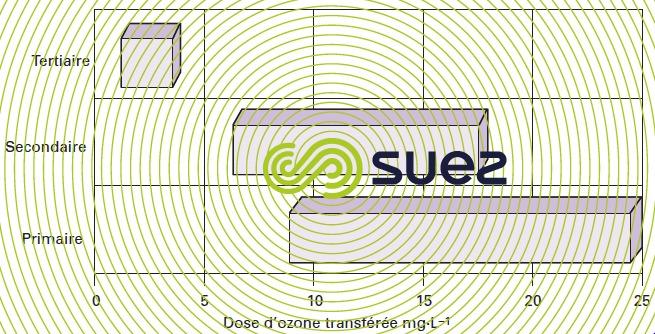
L’efficacité de désinfection est souvent évaluée en terme de dose d’ozone transférée pour l’inactivation des coliformes fécaux ou de E. coli. Elle augmente à mesure que la qualité de l’eau s’améliore au fil de la filière de traitement sous l’effet de la réduction des concentrations en autres composés oxydables. La figure 27 montre la dispersion des doses d’ozone suivant divers cas d’effluents primaires, secondaires ou tertiaires. Il est, en général, déraisonnable de traiter un effluent primaire, il faut au moins une bonne qualité secondaire (DBO < 20 mg · L–1 et MES < 20 mg · L–1) ou alors ne rechercher qu’un abattement faible de bactérie ou virus (inférieur à 2 log).


Dans les procédés de traitement à boues activées, l’injection d’ozone en dérivation réduit la production de boues (voir Biolysis O) tout en améliorant la qualité des flocs biologiques (voir réduction de production de boues). La réaction est rapide et nécessite un réacteur à forte agitation non conventionnel qui crée une forte aire d’échange.
Dans le traitement des boues biologiques en excès issues de la digestion anaérobie ou de la stabilisation aérobie, l’ozone améliore la déshydratation et l’épaississement des boues avec un effet bénéfique sur la production d’odeurs.
désodorisation et épuration des gaz
(voir ventilation et traitement des odeurs)
L’ozone est appliqué pour oxyder les composés soufrés (sulfures et mercaptans tels que sulfure d’hydrogène et méthyl mercaptan), des amines (par exemple, éthylamine et triméthylamine), des cétones, alcools et aldéhydes. Quelques cas de réalisations industrielles existent. Elles sont fondées sur l’emploi de tours de lavage consistant en des colonnes à garnissage dans lesquelles l’oxydation opère par voie humide (figure 20). Le temps de contact est de l’ordre de 3 secondes. Le pH de l’eau de lavage est régulé à 9-9,5 pour l’élimination des composés soufrés, des aldéhydes, des cétones et des alcools, à moins de 6,5 pour la destruction des amines. La dose d’ozone appliquée varie en moyenne de 6 à 12 mg · m–3 de gaz TPN.
piscines
L’ozone est utilisé à diverses étapes du traitement des eaux recyclées dans les centres nautiques :
- introduit à raison de 0,5 à 1 mg · L–1 dans le bac tampon en sortie du bassin, il oxyde des contaminants anthropogéniques (substances aminées) ;
- ultérieurement appliqué entre deux étapes de filtration, il assure l’oxydation des matières organiques résiduelles, il améliore ainsi les qualités visuelles et organoleptiques de l’eau et assure la désinfection ;
- injecté en amont du bassin, il constitue une barrière bactéricide et virulicide.
Les réacteurs utilisés sont en général des colonnes à bulles. Des systèmes à mélangeur statique peuvent convenir pour le traitement en amont de la filtration.
eaux résiduaires industrielles
Les applications de l’ozone pour le traitement des eaux résiduaires industrielles sont très variées ainsi qu’en témoigne la liste des installations en fonctionnement recensées, dressée au tableau 11. Les doses d’ozone mentionnées sont éminemment variables selon la cible visée et la qualité de l’eau à traiter.

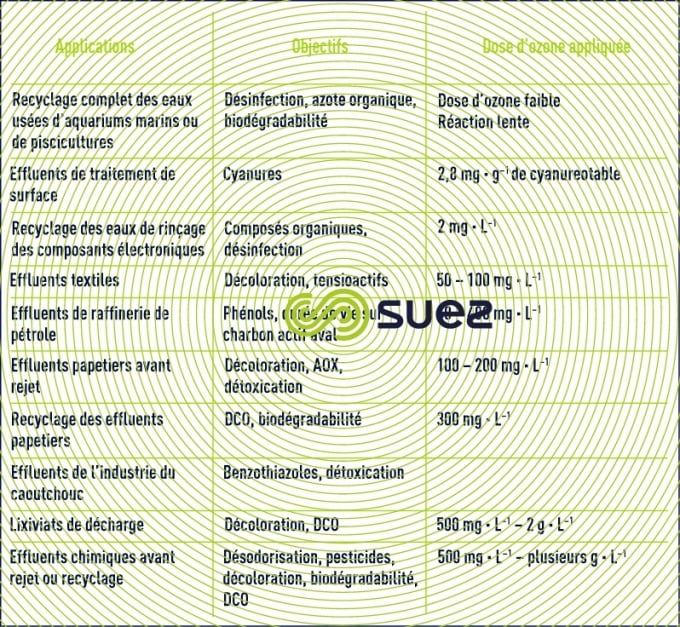

Pour chaque application, le réacteur est choisi en fonction des vitesses de réactions et de la qualité d’eau. C’est par exemple une colonne à garnissage sur une fraction du débit d’alimentation ou de recyclage en pisciculture pour la désinfection, un système avec mélangeur statique pour la décoloration d’eaux peu chargées ou un réacteur à diffuseur radial pour le traitement d’effluents avec temps de contact élevé (photo 12). Ils sont dimensionnés d’après étude cinétique menée en mode continu ou discontinu.



applications industrielles
La réactivité de l’ozone est mise à profit dans diverses étapes de production industrielle :
- blanchiment de la pâte à papier (voir industries de la pâte à papier et papeteries) ;
- purification (blanchiment) du kaolin et du carbonate de calcium ;
- synthèses chimiques, arômes, acides organiques… ;
- purification des acides sulfurique et phosphorique ;
- blanchiment du sucre de cannes.
- conditionnement de produits alimentaires
Outil Marque-page
Cliquez sur l'outil marque-page, puis surlignez le dernier paragraphe lu pour pouvoir poursuivre ultérieurement votre lecture.













