précipitation du silicium
Temps de lecture :Il s’agit en fait de l’adsorption de la silice sur un floc d’hydroxyde de Aℓ ou de Mg. Cette coprécipitation peut s’effectuer à froid ou à chaud. Elle est souvent réalisée simultanément avec celle du CaCO3 en décarbonatation.
désiliciage par Mg2+
Si le magnésium est présent dans les eaux de forage et si le pH est suffisant, il précipitera lors de leur décarbonatation avec une partie de la silice. Un appoint de Mg peut être effectué par de la poudre de MgO qui se solubilise par carbonatation en MgCO3 à froid. On peut également rajouter un sel de Mg, chlorure ou sulfate.

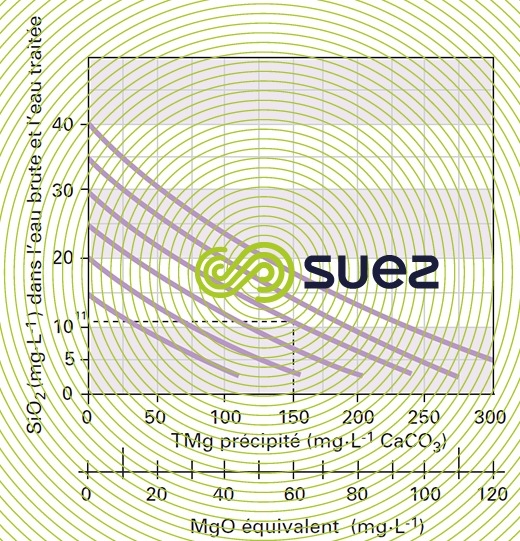

Selon les analyses de l’eau brute, la température et l’abattement recherché, des graphiques permettent le calcul de la dose de MgO (figure 6) réagissant et, par différence, celle à apporter.
Cette dose varie à froid de 3,2 à 1,8 mg de MgO par mg de SiO2 adsorbé, pour une concentration initiale de 20 à 40 mg · L–1.
Exemple :
- 150 mg · L–1 (en CaCO3) soit 15 °F de TMg précipités ;
- teneur en SiO2 de l’eau brute – 30 mg · L–1 ;
- teneur en SiO2 de l’eau traitée – 11 mg · L–1 ;
- Et si l’on recherche 8 mg · L–1 de SiO2 résiduelle il faudra ajouter au moins 25 mg · L–1 (en CaCO3) de Mg sous forme de réactifs.
désiliciage par l’aluminate de sodium
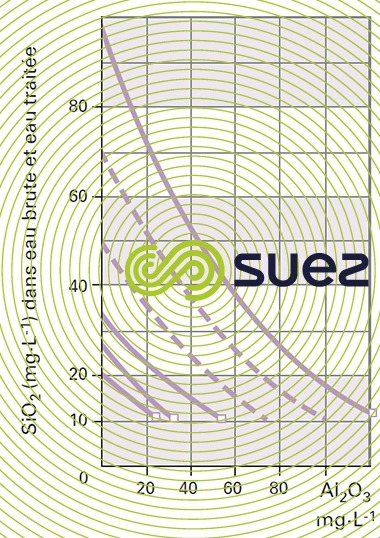
Ce traitement est de préférence effectué à froid (figure 7).
Les valeurs résiduelles obtenues sont plus élevées qu’avec MgO.
La dose d’aluminium exprimée en Aℓ2O3 est dans les eaux saumâtres de l’ordre de 2 à 2,6 mg par mg de silice coprécipitée.
En décarbonatation chaux-soude d’eau de forage, les taux résiduels de SiO2 obtenus ont les ordres de grandeur suivants pour des teneurs initiales de 20 à 40 mg · L–1 de silice (tableau 7) :
La teneur initiale de l’eau en Mg, les prix des réactifs et les volumes de boues produits déterminent le choix entre les deux réactifs.



Utilisation de FeCℓ3 :
L’utilisation de FeCℓ3 en combinaison avec l’aluminate permet d’obtenir un aluminium résiduel de 0,2 à 0,3 mg · L–1 à pH 8,5-9 au lieu de 3 mg · L–1 avec l’aluminate seul.


silice colloïdale
Bien que sa nature chimique soit variable, il s’agit le plus souvent de particules très fines (0,2 à 0,005 μm) d’argiles, parfois de silice polymérisée.
Les teneurs rencontrées sont de l’ordre de quelques mg · L–1 dans les eaux de rivière des pays tempérés, mais peuvent atteindre des dizaines de mg · L–1 dans certaines rivières tropicales, les lixiviats acides d’hydrométallurgie ou les eaux de formation pétrolière. Cette silice colloïdale n’étant pas ionisée, elle est mal éliminée par les chaînes traditionnelles de traitement des eaux de chaudières (clarification + échange d’ions) (voir traitement et conditionnement des eaux industrielles) et y pose de graves problèmes (entartrage, qualité vapeur…). Aussi, des méthodes complémentaires ont été mises au point :
- double floculation à 2 pH différents si possible pour des faibles valeurs (< 1 ou 2 mg · L–1) de silice colloïdale dans l’eau brute ;
- par filtration sur membrane d’ultrafiltration soit de l’eau clarifiée, soit de l’eau déminéralisée.
Outil Marque-page
Cliquez sur l'outil marque-page, puis surlignez le dernier paragraphe lu pour pouvoir poursuivre ultérieurement votre lecture.












